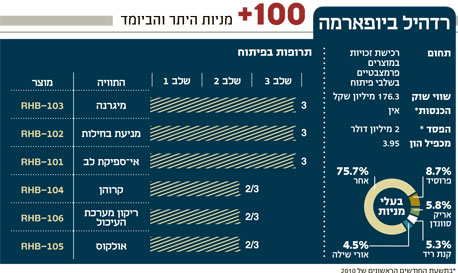
השורה התחתונה: ארבעת האתגרים שעומדים בדרכה של רדהיל אל מרשמי התרופות
המודל העסקי של רדהיל ביופארמה, המתבסס על שדרוג תרופות קיימות, מקצר את לוח הזמנים בדרך לקבלת אישור. אלא שדווקא התרופה שבעלת פוטנציאל השוק הגדול ביותר אכזבה בניסוי האחרון, ותרופות אחרות יותירו לחברה שולי רווח קטנים לאחר מסחור
לוח זמנים לפיתוח עסקי של חברות ביומד הוא דבר נזיל, ומתן תחזית ללו"ז שכזה יכולה להיות בעייתית, עקב גורמים קשים לחיזוי כמו הליכי ניסויים קליניים, דרישות רגולטוריות ויכולות גיוס הון.
רדהיל ביופארמה, שהונפקה לפני כחודש בבורסה בתל אביב, שואפת להגיש חמש משש התרופות שבפורטפוליו המוצרים שלה לאישור ה־FDA (מינהל המזון והתרופות האמריקאי) עד סוף שנת 2012. המוצר הראשון והמתקדם ביותר שלה, RHB-103 לטיפול במיגרנה, יוגש לפי התכנון לאישור עוד השנה.
להלכה, המודל העסקי של החברה תומך בלוחות הזמנים הקצרים שהציבה: בשונה מחברות אחרות בתחום מדעי החיים, המשקיעות חלק ניכר ממאמצי הפיתוח העסקי שלהן בחיפוש אחר שותפים אסטרטגיים, החברה בניהולו של דרור בן אשר מציגה את עצמה כשותף האסטרטגי לשלבי פיתוח קליניים מתקדמים ומסחור תרופות של חברות אחרות.
רדהיל מציעה עסקאות מסחור של תרופות מקור שיפותחו בהליך קליני קצר וזול המכונה 505b2, שבסופו מעניק ה־FDA תקופת בלעדיות של עד שלוש שנים. מסלול זה נועד בעיקר לתרופות שבהן החומר הפעיל כבר קיים בשוק, וחדשנות המוצר המבקש אישור באה לידי ביטוי באופן הנטילה, במינון ובשימושים נוספים.
אם רדהיל תשחק היטב עם הקלפים שברשותה, יכול מודל עסקי זה לשמש לה כמקפצה לרכישת זכויות על תרופות נוספות בעלות סיכויי הצלחה גבוהים בשווקים משמעותיים, ולבסס את דרכה העסקית. אלא שכאן בדיוק טמונה השאלה: האם תשכיל רדהיל להפיק את המיטב מהמודל העסקי שבחרה?
1.
תחרות בשוק צפוף
העובדה שרדהיל בחרה להשביח תרופות קיימות תקצר אמנם את מסלול הפיתוח והרגולציה עד לאישורן, אך בקצה הדרך מצפה לרדהיל תחרות קשה. למשל, תרופת RHB-101 שמיועדת לטיפול במחלות לב, תוך שחרור מבוקר של חומר פעיל גנרי בשם Carvedilol, מציעה שיפור לתרופות גנריות קיימות בכך שהיא מאפשרת נטילה אחת ליום (במקום שתיים).
רדהיל מתכננת להגיש את תיק התרופה ל־FDA במהלך 2012, ואישור יחשוף אותה לשוק של כחצי מיליארד דולר - אך קשה לראות כיצד תשיג בו נתח משמעותי לאור התחרות הצפופה.
כבר היום משווקת ענקית התרופות הבריטית GSK גרסה משופרת של תרופת ה־Coreg, אשר האריכה את משך פעילותה ואפשרה נטילה אחת ליום. הפטנט של GSK צפוי לפוג רק ב־2023, אך תחרות גנרית עשויה להתפתח כבר בקרוב, מצדה של מיוטורל פארמסוטיקל, שהגישה ב־2008 בקשה לאישור גרסה גנרית, והגיעה להסדר עם יצרנית תרופת המקור. תחרות גנרית עלולה לצמצם את השוק שאליו פונה רדהיל בכ־50%.
תחרות בעוצמה דומה צפויה לרדהיל גם בשוק שאליו פונות התרופות RHB-102 למניעת בחילות לאחר טיפולי כימותרפיה, ו־RHB-103 לטיפול במיגרנות.
2.
אורך חיי הפטנטים
מוצר נוסף בפורטפוליו של רדהיל הוא RHB-104 לטיפול בחולי קרוהן (מחלה דלקתית במערכת העיכול) הנגועים בחיידק ה־MAP. המוצר מציע קומבינציה מוגנת פטנט של שלושה חומרים אנטיביוטיים גנריים בקפסולה אחת - ונכון להיום, אין תרופה מאושרת מתחרה בהתוויה זו.
שוק היעד העולמי לתרופה מוערך על ידי רדהיל ב־2 מיליארד דולר. החברה עורכת בימים אלה הכנות לקראת ניסוי קליני שלב 2/3, הצפוי לעקוב אחר יותר מ־200 חולי קרוהן במשך יותר משנה.
רדהיל מצפה שכבר בשנת 2012 תוכל להגיש בקשה לאישור התרופה לשיווק (במסלול רגיל), אך גם אם תצלח את המסלול הזה, תתקשה להחזיק בבלעדיות השיווק למשך זמן רב, שכן כבר ב־2018 יפוג הפטנט שקיבלה על ה־RHB-104. עם זאת, הגישה רדהיל בקשה לפטנט נוסף, שעשויה, אם תאושר, לספק הגנה למוצר עד 2029.
הפטנט על תרופה אחרת, RHB-105 לטיפול בדלקות במערכת העיכול, יפוג ב־2019. רדהיל מקווה להגיש ל־FDA את המוצר לאישור במסלול רגיל ב־2013. אחרי 2019 תיאלץ להתמודד מול מתחרות גנריות.
3.
הטיפול שהציג הקלה בלבד
ביום שרדהיל תצטייד באישורים לשיווק התרופות, היא תזדקק ככל הנראה לסיוע של ענקיות פארמה בעלות יכולות מוכחות בשוקי היעד, אך פרט לתרופת RHB-104 לחולי קרוהן, בעלת פוטנציאל שוק של 2 מיליארד דולר, הסכם מסחור עם ענקית פארמה עשוי להותיר לה שולי רווח קטנים יחסית. לתרופה כמו RHB-101, למשל, שוק משוער של חצי מיליארד דולר, כך שרדהיל תהיה מרוצה אם תראה הכנסות שנתיות של 15 מיליון דולר ממנה.
אישור לשיווק תרופת RHB-104 עשוי, בניגוד לאחרים, להתברר כבוננזה, ורדהיל עשויה ליהנות מתמלוגים של כ־40% על המכירות (בדומה לתנאי ההסכם שחתמה חברת פרוטליקס עם פייזר לשיווק התרופה שפיתחה פרוטליקס לטיפול בחולי גושה).
עם זאת, קשה להעריך אם התרופה לטיפול בקרוהן תזכה, בסופו של דבר, לאישור ה־FDA. התרופה של רדהיל סיימה, אמנם, ניסוי שלב 3 באוסטרליה, אך הניסוי לא התמקד בחולים הנגועים בחיידק ה־MAP. בנוסף, החברה ביקשה להשיג אישור להתוויה של ריפוי הקרוהן, אולם בפועל, מתוצאות הניסוי עלה שהתרופה מספקת לחולים הפוגה או הקלה בלבד. נכון להיום, רדהיל אינה הציגה מידע קליני כלשהו שירמז על סיכויי ההצלחה של הטיפול בחיידק.
4.
הגיוס הבא בדרך
לפני כחודש הפתיעה רדהיל לאחר שוויתרה על המכרז המוסדי המקדים, ודילגה היישר למכרז הציבורי שבו גייסה 51.6 מיליון שקל - גבוה ב־29% מהסכום שביקשה לגייס (40 מיליון שקל). רדהיל נסחרת לפי שווי שוק של 176 מיליון שקל, ובמסחר אתמול ננעלה מנייתה במחיר של 3.42 שקלים - ירידה של 5.2% מהמחיר שנקבע במכרז.
מחיר מימוש האופציות (סדרה 1) שהוענקו במסגרת ההנפקה עומד על 3.8 שקלים, כך שעלייה של 11% במניה תכניס את האופציות לתוך הכסף. בהנחה שמלוא האופציות שהוענקו גם ימומשו, רדהיל עשויה להעשיר את קופתה בכ־25 מיליון שקל. כיום בקופתה של רדהיל כ־79 מיליון שקל, והחברה מקווה שסכום זה יספיק לה למימון ניסוי נוסף בתרופה לקרוהן.
ההוצאות התפעוליות של רדהיל מצומצמות, מאחר שהיא מעסיקה 11 עובדים בלבד (שש במשרה מלאה), וכל הפיתוח מבוצע במיקור חוץ. עם זאת, כדי לבסס את דרכה העסקית, תיאלץ החברה לצאת לעוד גיוסים, שישמשו אותה לרכישת רישיונות לתרופות נוספות.
השורה התחתונה: המודל העסקי, שנשען על הליך פיתוח קצר וזול, מגדיל את סיכויי ההצלחה של רדהיל, אבל תוצאות הניסויים הקליניים והתחרות הגנרית שמחכה למוצרים מציבות אתגר משמעותי בדרכה של החברה.
תגובה אחת לכתיבת תגובה